摘要:日本理研研究所的研究人員發現了蛋白質合成與神經發育障礙之間的聯系,發現蛋白質生產過程中過度活躍的質量控制過程會抑制神經生長和交流,導致認知功能障礙。這為治療這類疾病開辟了潛在的新途徑。
日本理化研究所的研究人員現在已經發現了核糖體相關質量控制失調與認知障礙之間的聯系。當蛋白質合成停滯時的過度反應會導致小鼠神經發育障礙。
細胞內復雜的分子工廠,核糖體將遺傳密碼轉化為蛋白質分子。這種蛋白質合成斷斷續續地進行,有時會完全停止。當這種情況發生時,一個重要的質量控制過程就會啟動,并降解已經形成的不完整的蛋白線,否則這些蛋白線會損害細胞。這種清除操作被稱為核糖體相關質量控制(RQC)。
最近,有一些證據表明,當RQC出錯時,會導致各種大腦疾病,但沒有人知道這是如何發生的。日本理化研究所的研究人員首次明確了細胞中蛋白質合成過程中的質量控制與神經系統疾病之間的聯系。這一發現可能有助于開發針對這類認知障礙的新療法。

圖1 研究人員首次明確了細胞中蛋白質合成過程中的質量控制與神經系統疾病之間的聯系
“以前的研究表明,RQC的功能障礙可能導致神經退行性疾病,”RIKEN腦科學中心的Motomasa Tanaka說。“所以我們真的對神經元中發生的事情很感興趣,但到目前為止,大多數研究都集中在培養細胞系或酵母細胞上,而不是神經元上。”
Ryo Endo、Tanaka和同事們發現,去除小鼠神經元中RQC中的一個關鍵基因會導致神經元發育缺陷。
具體來說,研究小組發現,缺乏LTN1酶的小鼠具有更高水平的兩種信號分子:TTC3和UFMylation。“蛋白質TTC3的豐度增加了十倍以上,”Tanaka指出。“這真的很令人驚訝,因為這是一種過度殺傷。”這些信號分子的作用是阻止遺傳物質轉化為蛋白質——這是一種有益的作用。但它們走得太遠了,阻礙了神經突的生長,神經突是神經元的突起,然后與其他神經元形成連接。正是這種對神經突的抑制被認為導致了神經元的問題。
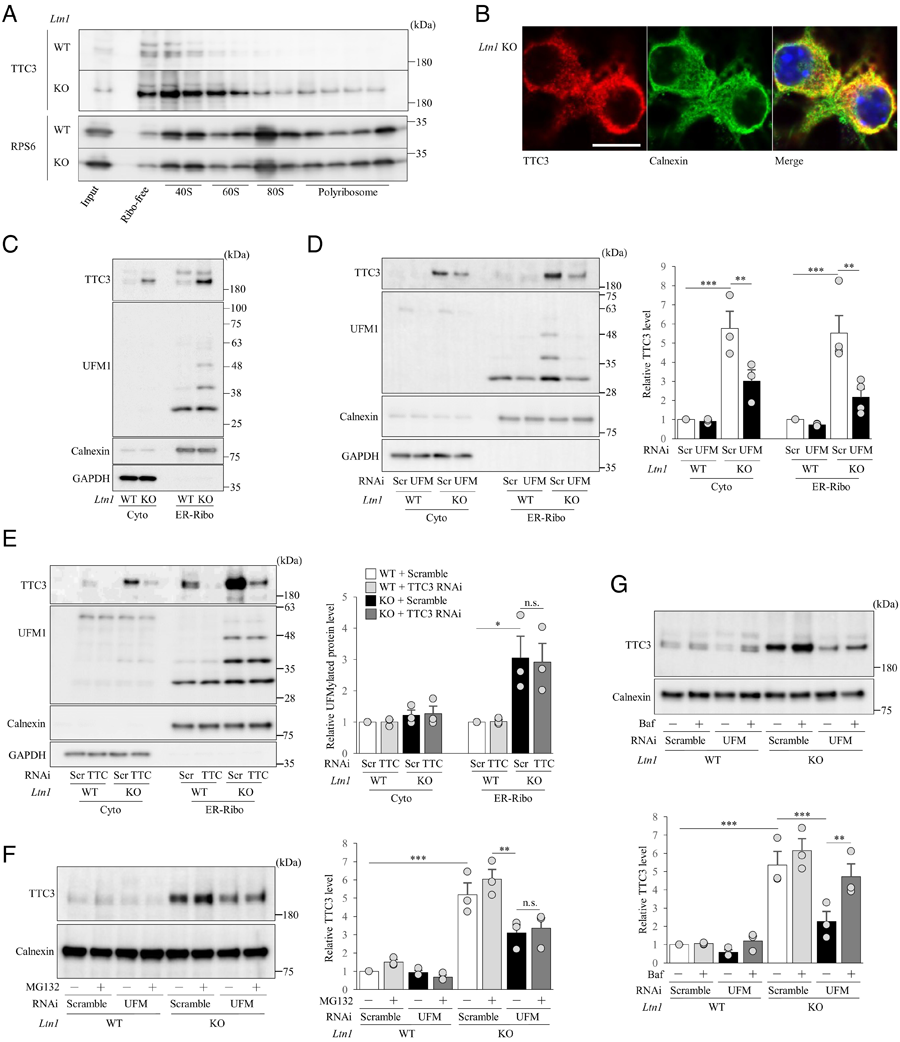
圖2 TTC3蛋白在Ltn1 KO神經元的40S亞單位中積累
Tanaka說:“TTC3的過度表達肯定有助于阻止翻譯,這是一件好事。但與此同時,它也抑制了神經突的延伸,減少了神經元之間的交流。這可能是導致認知功能障礙的原因。”
過度補償免疫系統過度活躍的初始問題,可能導致慢性炎癥和過敏等嚴重疾病。
這一發現可能有助于開發新的治療方法。Tanaka說:“我們認為一些針對TTC3或照明信號因子的治療策略在未來也會很有趣。”
該團隊現在打算探索信號功能障礙的積累與人類大腦疾病之間的關系。
參考資料:
[1] “Dysregulation of ribosome-associated quality control elicits cognitive disorders via overaccumulation of TTC3” by Ryo Endo, Yi-Kai Chen, John Burke, Noriko Takashima, Nayan Suryawanshi, Kelvin K. Hui, Tatsuhiko Miyazaki and Motomasa Tanaka, 14 March 2023, Proceedings of the National Academy of Sciences.
摘要:日本理研研究所的研究人員發現了蛋白質合成與神經發育障礙之間的聯系,發現蛋白質生產過程中過度活躍的質量控制過程會抑制神經生長和交流,導致認知功能障礙。這為治療這類疾病開辟了潛在的新途徑。
日本理化研究所的研究人員現在已經發現了核糖體相關質量控制失調與認知障礙之間的聯系。當蛋白質合成停滯時的過度反應會導致小鼠神經發育障礙。
細胞內復雜的分子工廠,核糖體將遺傳密碼轉化為蛋白質分子。這種蛋白質合成斷斷續續地進行,有時會完全停止。當這種情況發生時,一個重要的質量控制過程就會啟動,并降解已經形成的不完整的蛋白線,否則這些蛋白線會損害細胞。這種清除操作被稱為核糖體相關質量控制(RQC)。
最近,有一些證據表明,當RQC出錯時,會導致各種大腦疾病,但沒有人知道這是如何發生的。日本理化研究所的研究人員首次明確了細胞中蛋白質合成過程中的質量控制與神經系統疾病之間的聯系。這一發現可能有助于開發針對這類認知障礙的新療法。

圖1 研究人員首次明確了細胞中蛋白質合成過程中的質量控制與神經系統疾病之間的聯系
“以前的研究表明,RQC的功能障礙可能導致神經退行性疾病,”RIKEN腦科學中心的Motomasa Tanaka說。“所以我們真的對神經元中發生的事情很感興趣,但到目前為止,大多數研究都集中在培養細胞系或酵母細胞上,而不是神經元上。”
Ryo Endo、Tanaka和同事們發現,去除小鼠神經元中RQC中的一個關鍵基因會導致神經元發育缺陷。
具體來說,研究小組發現,缺乏LTN1酶的小鼠具有更高水平的兩種信號分子:TTC3和UFMylation。“蛋白質TTC3的豐度增加了十倍以上,”Tanaka指出。“這真的很令人驚訝,因為這是一種過度殺傷。”這些信號分子的作用是阻止遺傳物質轉化為蛋白質——這是一種有益的作用。但它們走得太遠了,阻礙了神經突的生長,神經突是神經元的突起,然后與其他神經元形成連接。正是這種對神經突的抑制被認為導致了神經元的問題。

圖2 TTC3蛋白在Ltn1 KO神經元的40S亞單位中積累
Tanaka說:“TTC3的過度表達肯定有助于阻止翻譯,這是一件好事。但與此同時,它也抑制了神經突的延伸,減少了神經元之間的交流。這可能是導致認知功能障礙的原因。”
過度補償免疫系統過度活躍的初始問題,可能導致慢性炎癥和過敏等嚴重疾病。
這一發現可能有助于開發新的治療方法。Tanaka說:“我們認為一些針對TTC3或照明信號因子的治療策略在未來也會很有趣。”
該團隊現在打算探索信號功能障礙的積累與人類大腦疾病之間的關系。
參考資料:
[1] “Dysregulation of ribosome-associated quality control elicits cognitive disorders via overaccumulation of TTC3” by Ryo Endo, Yi-Kai Chen, John Burke, Noriko Takashima, Nayan Suryawanshi, Kelvin K. Hui, Tatsuhiko Miyazaki and Motomasa Tanaka, 14 March 2023, Proceedings of the National Academy of Sciences.



