摘要:研究人員揭示了包括SARS-CoV-2、SARS-CoV-1和MERS-CoV在內(nèi)的冠狀病毒如何利用一種稱為“半胱氨酸天冬氨酸蛋白酶6”(Caspase-6)的宿主蛋白酶進(jìn)行有效復(fù)制的機(jī)制。
冠狀病毒的核糖核酸(RNA)進(jìn)入宿主細(xì)胞后,會(huì)觸發(fā)感染細(xì)胞分泌干擾素,抑制病毒在感染細(xì)胞內(nèi)復(fù)制,降低其他未感染細(xì)胞之間的感染風(fēng)險(xiǎn)。同時(shí),宿主細(xì)胞也會(huì)發(fā)生凋亡過程,即程序化的細(xì)胞死亡過程,使細(xì)胞不再成為病毒復(fù)制的工廠。因此,干擾素反應(yīng)和細(xì)胞凋亡是人類和動(dòng)物細(xì)胞中很重要的抗病毒機(jī)制。
細(xì)胞凋亡是由半胱氨酸-天冬氨酸蛋白酶在人和動(dòng)物細(xì)胞中執(zhí)行的,通過該蛋白酶清除感染細(xì)胞以抑制病毒復(fù)制。香港大學(xué)醫(yī)學(xué)院的研究小組研究了caspase-6在一系列細(xì)胞系、人離體肺組織、人腸道類器官和動(dòng)物模型中對(duì)冠狀病毒復(fù)制的影響。研究小組發(fā)現(xiàn),caspase-6的化學(xué)抑制或基因缺失顯著降低了冠狀病毒的復(fù)制,而過表達(dá)caspase-6有效地促進(jìn)了冠狀病毒的復(fù)制。
圖1 caspase-6在一系列細(xì)胞系、人離體肺組織、人腸道類器官和動(dòng)物模型中對(duì)冠狀病毒復(fù)制的影響(圖源:[1])
研究方法和結(jié)果
在小鼠模型中,caspase-6的化學(xué)抑制劑極大地限制了小鼠適應(yīng)的MERS-CoV (MERS-CoVMA)的復(fù)制,并顯著地將小鼠的存活率從33.3%提高到80%。此外,在caspase-6敲除小鼠的肺中,MERS-CoVMA復(fù)制和MERS-CoVMA誘導(dǎo)的肺損傷明顯減少。同樣,在倉(cāng)鼠模型中,針對(duì)caspase-6的特異性化學(xué)抑制劑減少了SARS-CoV-2的復(fù)制和相關(guān)的炎癥性肺損傷。
但冠狀病毒如何利用caspase-6來造福自己呢?請(qǐng)注意,干擾素反應(yīng)是宿主細(xì)胞重要和直接的抗病毒防御。我們的進(jìn)一步研究發(fā)現(xiàn),caspase-6可以切割冠狀病毒核衣殼(N)蛋白,產(chǎn)生N個(gè)片段,與宿主的“干擾素調(diào)控因子3 (IRF3)”相互作用,阻止其進(jìn)入細(xì)胞核啟動(dòng)干擾素應(yīng)答。因此,病毒N片段作為干擾素拮抗劑,促進(jìn)病毒復(fù)制。
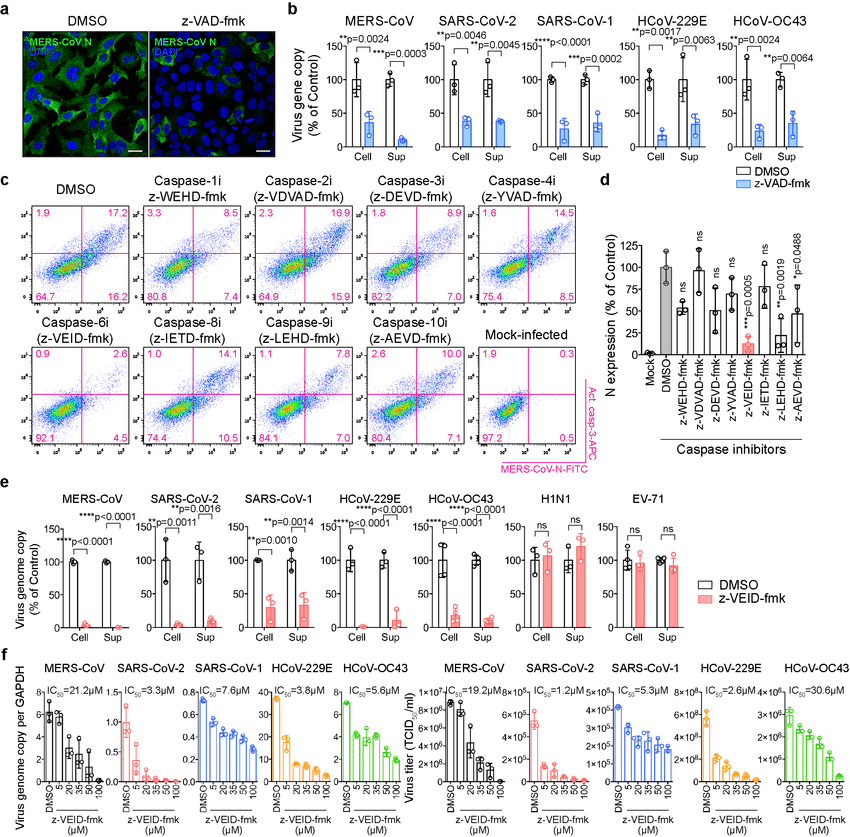
圖2 在小鼠模型中,caspase-6的化學(xué)抑制劑極大地限制了小鼠適應(yīng)的MERS-CoV (MERS-CoVMA)的復(fù)制(圖源:[1])
研究意義
這項(xiàng)研究顯示了冠狀病毒是如何進(jìn)化成很成功的病原體的。我們揭示了冠狀病毒如何克服宿主細(xì)胞對(duì)干擾素反應(yīng)的抗病毒防御的一種新機(jī)制,通過開發(fā)一類新的宿主蛋白酶,caspase-6,該蛋白酶原本是宿主用來執(zhí)行細(xì)胞凋亡,作為一種防御病毒感染,以獲得更好的病毒復(fù)制。這些結(jié)果進(jìn)一步表明,可以設(shè)計(jì)針對(duì)caspase-6的藥物,它可以成為所有已知人類冠狀病毒感染抗病毒治療的潛在干預(yù)目標(biāo)。
參考資料:
[1] Hin Chu, Yuxin Hou, Dong Yang, Lei Wen, Huiping Shuai, Chaemin Yoon, Jialu Shi, Yue Chai, Terrence Tsz-Tai Yuen, Bingjie Hu, Cun Li, Xiaoyu Zhao, Yixin Wang, Xiner Huang, Kin Shing Lee, Luo Cuiting, Jian-Piao Cai, Vincent Kwok-Man Poon, Chris Chung-Sing Chan, Anna Jinxia Zhang, Shuofeng Yuan, Ko-Yung Sit, Dominic Chi-Chung Foo, Wing-Kuk Au, Kenneth Kak-Yuen Wong, Jie Zhou, Kin-Hang Kok, Dong-Yan Jin, Jasper Fuk-Woo Chan, Kwok-Yung Yuen. Coronaviruses exploit a host cysteine-aspartic protease for replication. Nature, 2022
摘要:研究人員揭示了包括SARS-CoV-2、SARS-CoV-1和MERS-CoV在內(nèi)的冠狀病毒如何利用一種稱為“半胱氨酸天冬氨酸蛋白酶6”(Caspase-6)的宿主蛋白酶進(jìn)行有效復(fù)制的機(jī)制。
冠狀病毒的核糖核酸(RNA)進(jìn)入宿主細(xì)胞后,會(huì)觸發(fā)感染細(xì)胞分泌干擾素,抑制病毒在感染細(xì)胞內(nèi)復(fù)制,降低其他未感染細(xì)胞之間的感染風(fēng)險(xiǎn)。同時(shí),宿主細(xì)胞也會(huì)發(fā)生凋亡過程,即程序化的細(xì)胞死亡過程,使細(xì)胞不再成為病毒復(fù)制的工廠。因此,干擾素反應(yīng)和細(xì)胞凋亡是人類和動(dòng)物細(xì)胞中重要的抗病毒機(jī)制。
細(xì)胞凋亡是由半胱氨酸-天冬氨酸蛋白酶在人和動(dòng)物細(xì)胞中執(zhí)行的,通過該蛋白酶清除感染細(xì)胞以抑制病毒復(fù)制。香港大學(xué)醫(yī)學(xué)院的研究小組研究了caspase-6在一系列細(xì)胞系、人離體肺組織、人腸道類器官和動(dòng)物模型中對(duì)冠狀病毒復(fù)制的影響。研究小組發(fā)現(xiàn),caspase-6的化學(xué)抑制或基因缺失顯著降低了冠狀病毒的復(fù)制,而過表達(dá)caspase-6有效地促進(jìn)了冠狀病毒的復(fù)制。

圖1 caspase-6在一系列細(xì)胞系、人離體肺組織、人腸道類器官和動(dòng)物模型中對(duì)冠狀病毒復(fù)制的影響(圖源:[1])
研究方法和結(jié)果
在小鼠模型中,caspase-6的化學(xué)抑制劑極大地限制了小鼠適應(yīng)的MERS-CoV (MERS-CoVMA)的復(fù)制,并顯著地將小鼠的存活率從33.3%提高到80%。此外,在caspase-6敲除小鼠的肺中,MERS-CoVMA復(fù)制和MERS-CoVMA誘導(dǎo)的肺損傷明顯減少。同樣,在倉(cāng)鼠模型中,針對(duì)caspase-6的特異性化學(xué)抑制劑減少了SARS-CoV-2的復(fù)制和相關(guān)的炎癥性肺損傷。
但冠狀病毒如何利用caspase-6來造福自己呢?請(qǐng)注意,干擾素反應(yīng)是宿主細(xì)胞重要和直接的抗病毒防御。我們的進(jìn)一步研究發(fā)現(xiàn),caspase-6可以切割冠狀病毒核衣殼(N)蛋白,產(chǎn)生N個(gè)片段,與宿主的“干擾素調(diào)控因子3 (IRF3)”相互作用,阻止其進(jìn)入細(xì)胞核啟動(dòng)干擾素應(yīng)答。因此,病毒N片段作為干擾素拮抗劑,促進(jìn)病毒復(fù)制。

圖2 在小鼠模型中,caspase-6的化學(xué)抑制劑極大地限制了小鼠適應(yīng)的MERS-CoV (MERS-CoVMA)的復(fù)制(圖源:[1])
研究意義
這項(xiàng)研究顯示了冠狀病毒是如何進(jìn)化成很成功的病原體的。我們揭示了冠狀病毒如何克服宿主細(xì)胞對(duì)干擾素反應(yīng)的抗病毒防御的一種新機(jī)制,通過開發(fā)一類新的宿主蛋白酶,caspase-6,該蛋白酶原本是宿主用來執(zhí)行細(xì)胞凋亡,作為一種防御病毒感染,以獲得更好的病毒復(fù)制。這些結(jié)果進(jìn)一步表明,可以設(shè)計(jì)針對(duì)caspase-6的藥物,它可以成為所有已知人類冠狀病毒感染抗病毒治療的潛在干預(yù)目標(biāo)。
參考資料:
[1] Hin Chu, Yuxin Hou, Dong Yang, Lei Wen, Huiping Shuai, Chaemin Yoon, Jialu Shi, Yue Chai, Terrence Tsz-Tai Yuen, Bingjie Hu, Cun Li, Xiaoyu Zhao, Yixin Wang, Xiner Huang, Kin Shing Lee, Luo Cuiting, Jian-Piao Cai, Vincent Kwok-Man Poon, Chris Chung-Sing Chan, Anna Jinxia Zhang, Shuofeng Yuan, Ko-Yung Sit, Dominic Chi-Chung Foo, Wing-Kuk Au, Kenneth Kak-Yuen Wong, Jie Zhou, Kin-Hang Kok, Dong-Yan Jin, Jasper Fuk-Woo Chan, Kwok-Yung Yuen. Coronaviruses exploit a host cysteine-aspartic protease for replication. Nature, 2022



