一直以來(lái)大家都默認(rèn)基因都是在染色體上,染色體外DNA(ecDNA)這一概念的出現(xiàn)可以說(shuō)是顛覆了大家的傳統(tǒng)認(rèn)知,原來(lái)研究了半天,竟是搞錯(cuò)了方向,癌基因其實(shí)并不在我們關(guān)注的染色體上。由此,癌癥研究打開(kāi)了一扇新大門(mén)。
ecDNA是一種存在于染色體外,高度開(kāi)放的DNA 顆粒,普遍存在于人類(lèi)癌細(xì)胞中。因其能通過(guò)基因擴(kuò)增和改變基因調(diào)控來(lái)介導(dǎo)癌基因的高表達(dá),被認(rèn)為與腫瘤的異質(zhì)性和耐藥性相關(guān)。
編碼致癌基因的ecDNA是癌癥基因組的普遍特征,也是癌癥進(jìn)展的一個(gè)強(qiáng)有力的驅(qū)動(dòng)因素。ecDNA是共價(jià)閉合雙鏈,大小從100千堿基到幾兆堿基不等。因缺乏著絲粒,ecDNA在細(xì)胞分裂過(guò)程中會(huì)隨機(jī)分布于子細(xì)胞,這就方便了其快速積累,而且可以重新整合到染色體中,因此也可作為某些染色體擴(kuò)增的前體。ecDNA具有更高的染色質(zhì)可及性,但卻缺乏更高的染色質(zhì)致密性,且包含內(nèi)源性致癌基因增強(qiáng)子元件,這表明癌基因擴(kuò)增子可能是通過(guò)調(diào)控依賴(lài)性來(lái)擴(kuò)增轉(zhuǎn)錄的。因其本身存在于染色體外,目前對(duì)其細(xì)胞核中的空間還不清楚。ecDNA在細(xì)胞分裂期間或DNA損傷后會(huì)相互聚集,但其聚集后生物學(xué)后果目前還不甚了解。
11月24日,斯坦福大學(xué)HowardChang教授團(tuán)隊(duì)在《Nature》發(fā)表了題為“
ecDNAhubs drive cooperative intermolecular oncogene expression”的論文,他們研究了致癌ecDNA的細(xì)胞核空間、表觀遺傳因子和轉(zhuǎn)錄調(diào)控,發(fā)現(xiàn)聚集在間期細(xì)胞核中的ecDNA可以“抱團(tuán)行動(dòng)”,驅(qū)動(dòng)分子間增強(qiáng)子信號(hào)來(lái)促使癌基因表達(dá)擴(kuò)增。

ecDNA促進(jìn)癌癥基因表達(dá)
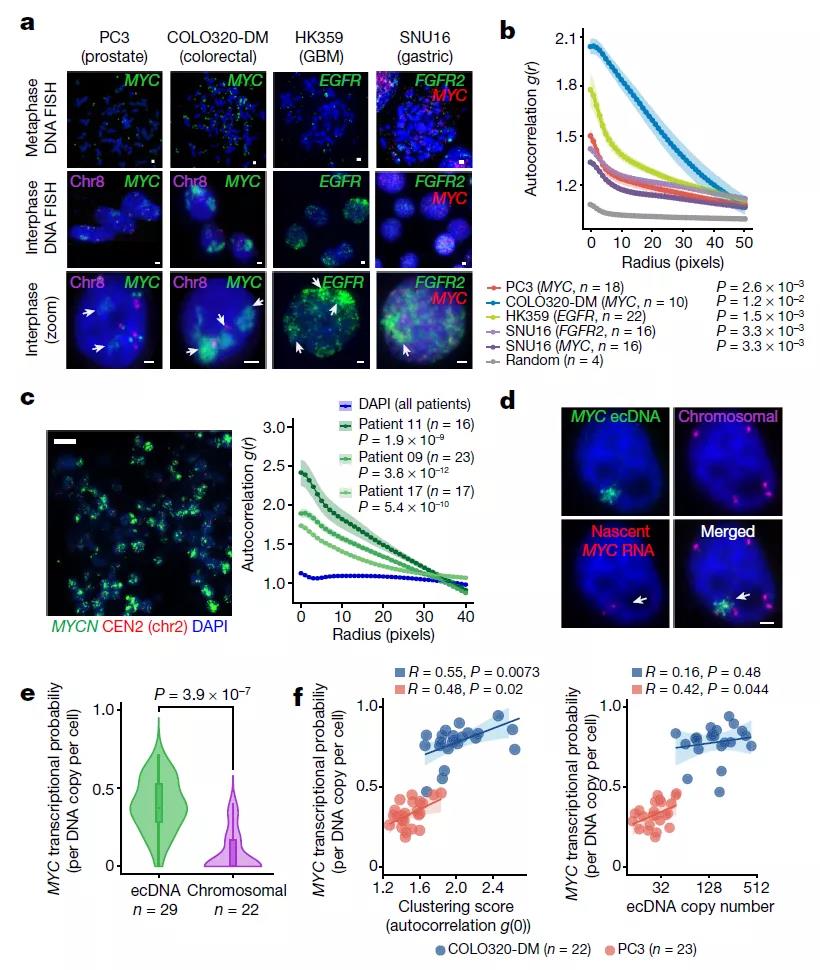
研究團(tuán)隊(duì)通過(guò)DNA熒光原位雜交(FISH)來(lái)觀察間期細(xì)胞核中的ecDNA的聚集點(diǎn),包括前列腺癌細(xì)胞系PC3(MYC擴(kuò)增)、結(jié)直腸癌細(xì)胞系COLO320-DM(MYC擴(kuò)增)、多形性成膠質(zhì)細(xì)胞瘤細(xì)胞系HK359(EGFR擴(kuò)增)和胃癌細(xì)胞系SNU16(MYC和FGFR2擴(kuò)增)。結(jié)果顯示,所有ecDNA陽(yáng)性癌細(xì)胞中,除去有數(shù)十到數(shù)百個(gè)單獨(dú)的ecDNA分子,ecDNAFISH基本都集中在間期細(xì)胞核中,這表明ecDNA彼此之間有強(qiáng)烈的聚集,研究團(tuán)隊(duì)將其稱(chēng)為ecDNA中心。進(jìn)一步實(shí)驗(yàn)后發(fā)現(xiàn),在具有不同癌基因擴(kuò)增的各種癌癥類(lèi)型和原發(fā)性腫瘤中均存在ecDNA聚集。
研究人員利用DNA和新生RNAFISH,在PC3和COLO320-DM細(xì)胞中觀察到活躍轉(zhuǎn)錄的MYC等位基因,并計(jì)算出每個(gè)ecDNA分子的MYC轉(zhuǎn)錄概率。大多數(shù)新生MYCmRNA轉(zhuǎn)錄本來(lái)自ecDNA中心,而不是來(lái)自染色體。此外,與單子ecDNA相比,ecDNA中心的轉(zhuǎn)錄活性更高。因此,ecDNAs中心聚集時(shí),每個(gè)ecDNA分子更有可能轉(zhuǎn)錄致癌基因
BRD4連接ecDNA中心和轉(zhuǎn)錄
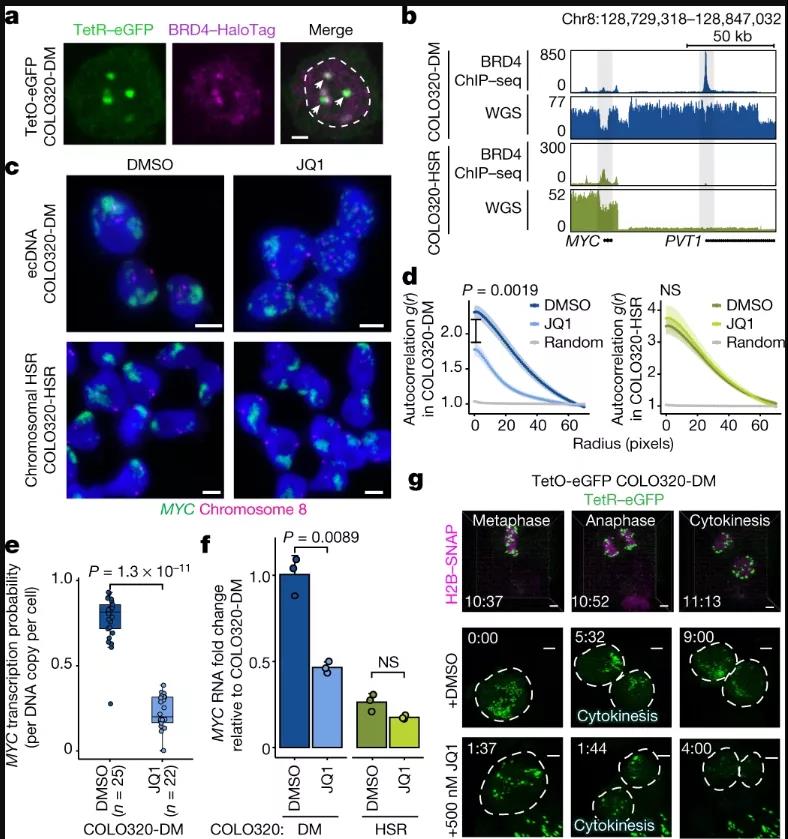
癌基因MYC包含MYC和漿細(xì)胞瘤轉(zhuǎn)化遷移基因1(PVT1,拷貝數(shù)擴(kuò)增相關(guān)的lncRNA,已知的癌癥相關(guān)區(qū)域),兩側(cè)是由組蛋白H3乙酰化賴(lài)氨酸27(H3K27ac)和BET蛋白(如BRD4)為標(biāo)記的超級(jí)增強(qiáng)因子。為了檢查活細(xì)胞中的MYCecDNA,研究人員在COLO320-DM細(xì)胞的MYCecDNA中插入了Tet-operator(TetO)陣列,并用Tet-eGFP標(biāo)記了ecDNA,以盡量減少GFP二聚化。活細(xì)胞成像顯示,有多個(gè)動(dòng)態(tài)核病灶對(duì)應(yīng)ecDNA聚集。內(nèi)源性BRD4的表位標(biāo)記顯示,BRD4在TetO標(biāo)記的ecDNA中心高度富集。通過(guò)對(duì)H3K27ac和BRD4進(jìn)行測(cè)序和染色質(zhì)免疫沉淀來(lái)分析染色質(zhì),結(jié)果顯示標(biāo)記活性H3K27ac的ecDNA也被BRD4占據(jù)。
為了確定BET蛋白在ecDNA相關(guān)轉(zhuǎn)錄中的作用,研究人員重點(diǎn)研究了同源的結(jié)直腸癌細(xì)胞系COLO320-DM(MYCecDNA)和COLO320-HSR(來(lái)源于同一患者腫瘤)。TetO-GFPCOLO320-DM細(xì)胞中進(jìn)行的活細(xì)胞成像顯示,ecDNA中心在有絲分裂過(guò)程中被分解成更小的顆粒。分解后,ecDNAs又再次聚集成大中心。值得注意的是,有絲分裂后,ecDNA中心重新聚集被JQ1(BRD4抑制劑)阻斷。結(jié)果表明,在COLO320-DM細(xì)胞中,ecDNA中心的形成、維持和腫瘤基因轉(zhuǎn)錄對(duì)BET蛋白H3K27ac相互作用有獨(dú)特的依賴(lài)性。
ecDNA中心反式激活
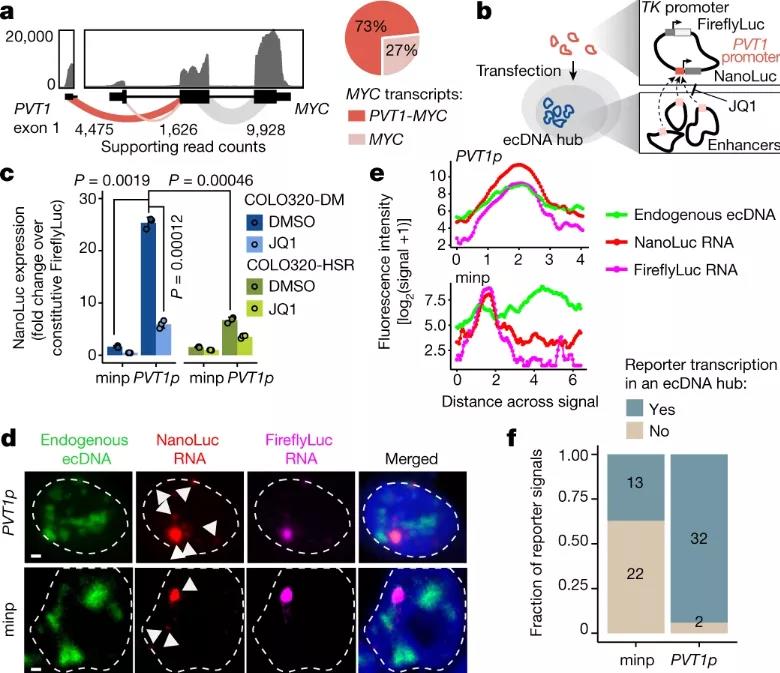
為了將ecDNA結(jié)構(gòu)與MYC轉(zhuǎn)錄調(diào)控聯(lián)系起來(lái),研究團(tuán)隊(duì)使用五種正交方法重建了COLO320-DM的ecDNA,報(bào)告了目前已知的組裝的大的ecDNA結(jié)構(gòu),包含PVT1-MYC融合、標(biāo)準(zhǔn)MYC序列和來(lái)自多個(gè)染色體起源的序列(6、8、13和16號(hào)染色體)的多個(gè)拷貝,并且利用DNA FISH驗(yàn)證了PLUT、PCAT1和MYC基因在重建預(yù)測(cè)的ecDNA上的共定位。
研究團(tuán)隊(duì)在COLO320-DM細(xì)胞中觀察到了PVT1啟動(dòng)子處的強(qiáng)BRD4結(jié)合,但在COLO320-DMecDNA細(xì)胞中未觀察到。因PVT1啟動(dòng)子能被MYC激活,研究團(tuán)隊(duì)又假設(shè)PVT1-MYC融合可實(shí)現(xiàn)MYC表達(dá)的正反饋,避免PVT1和MYC啟動(dòng)子之間的過(guò)度表達(dá),但在幾種人類(lèi)癌癥中觀察到了PVT1重排和基因融合并驅(qū)動(dòng)基因過(guò)度表達(dá)。
接下來(lái),研究人員確定了與癌基因高表達(dá)相關(guān)的ecDNA調(diào)控元件。72049個(gè)來(lái)自COLO320-DM和COLO320-HSR細(xì)胞的配對(duì)單細(xì)胞ATAC–seq和RNA-seq,經(jīng)校正MYC拷貝數(shù)后確定了47個(gè)與高M(jìn)YC表達(dá)相關(guān)的ecDNA調(diào)控元件,而目前驅(qū)動(dòng)ecDNA上MYC癌基因表達(dá)的PVT1啟動(dòng)子(PVT1p)在ecDNA中心內(nèi)接受了廣泛的組合增強(qiáng)子輸入。進(jìn)一步實(shí)驗(yàn)表明,分子間增強(qiáng)子-啟動(dòng)子在ecDNA中心激活,同時(shí)研究人員證實(shí)PVT1p作為一種DNA元件,能夠反式激活ecDNA中心。
ecDNA間的分子調(diào)控
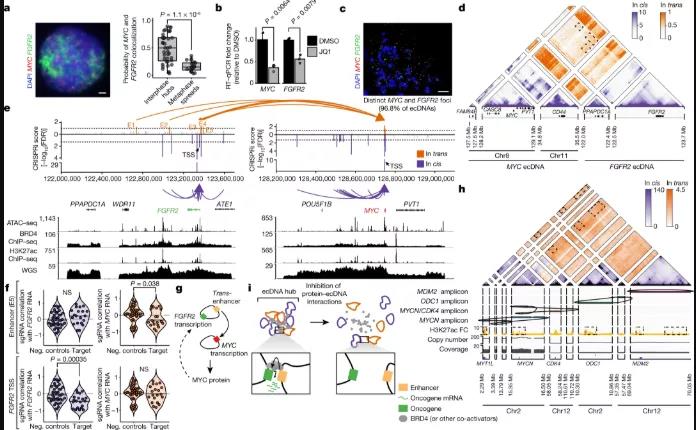
研究人員進(jìn)一步研究了分子間增強(qiáng)子-基因相互作用是如何進(jìn)行精確定位和干擾。以人胃癌細(xì)胞系SNU16為研究對(duì)象,其包含8號(hào)和11號(hào)染色體的MYC擴(kuò)增子和10號(hào)染色體的成纖維細(xì)胞生長(zhǎng)因子受體2(FGFR2)擴(kuò)增子。H3K27ac的染色質(zhì)免疫沉淀和測(cè)序顯示FGFR2和MYCecDNA之間存在分子間接觸,并富集了焦點(diǎn)相互作用。CRISPR干擾(CRISPRi)靶向候選調(diào)控元件確定了與MYC或FGFR2在順式和反式表達(dá)相關(guān)的功能元件。
實(shí)驗(yàn)結(jié)果表明,F(xiàn)GFR2和MYCecDNA已被共同選擇,因此這兩個(gè)擴(kuò)增子上的增強(qiáng)子可協(xié)同激活MYC表達(dá)。MYC蛋白繼而激活FGFR2表達(dá)。順式和反式調(diào)控元件之間幾乎沒(méi)有重疊,表明分子間增強(qiáng)子元件是直接修飾反式基因表達(dá),而非通過(guò)下游效應(yīng)。癌癥類(lèi)型中的分子間ecDNA的相互作用評(píng)估顯示,ecDNA中心的分子間增強(qiáng)子-基因激活發(fā)生在不同的腫瘤基因位點(diǎn)和多種癌癥類(lèi)型。
綜上所述,上述研究顯示ecDNA“抱團(tuán)行動(dòng)”促進(jìn)了新的分子間增強(qiáng)子-基因相互作用和癌基因過(guò)表達(dá),且可以發(fā)生在不同的腫瘤基因位點(diǎn)和多種癌癥類(lèi)型中。與傳統(tǒng)的順式染色體轉(zhuǎn)錄不同,ecDNA中心反式調(diào)控能夠?qū)崿F(xiàn)分子間轉(zhuǎn)錄調(diào)控,這對(duì)如何實(shí)現(xiàn)更好的癌基因轉(zhuǎn)錄具有重要的啟示。



