摘要:研究團隊開發(fā)出一種方法,可以預(yù)測哪些患者不會對常用的化療藥物產(chǎn)生應(yīng)答。
化療是摧毀腫瘤細胞的一種策略。幾十年來,它一直是治療癌癥的標準方法。然而,化療并非總是有效。
西班牙國家癌癥研究中心(CNIO)計算腫瘤學(xué)團隊負責人Geoff Macintyre解釋說:“化療對某些患者有效,但并非適用于所有病例。20%到50%的癌癥患者對這些藥物沒有應(yīng)答。他們將承受化療帶來的副作用,卻無法獲得任何臨床收益。”
 圖1 利用染色體不穩(wěn)定性特征預(yù)測化療耐藥性
圖1 利用染色體不穩(wěn)定性特征預(yù)測化療耐藥性Macintyre領(lǐng)導(dǎo)的研究團隊與劍橋大學(xué)和初創(chuàng)公司Tailor Bio合作,開發(fā)出一種方法,可以預(yù)測哪些患者不會對常用的化療藥物(如鉑類、紫杉類和蒽環(huán)類化療藥物)產(chǎn)生應(yīng)答。
這項研究成果于6月23日發(fā)表在《Nature Genetics》雜志上。
作者表示: “重要的是,我們的研究為多種藥物引入了患者分層的生物標志物,這些藥物原本并不是作為靶向療法開發(fā)的。”
共同第一作者、西班牙國家癌癥研究中心的Joe Sneath Thompson表示:“我們的基因組檢測可以定量三種化療藥物的生物標志物。該檢測適用于多種不同類型的癌癥,因此,我們的研究成果每年有望惠及數(shù)十萬名患者。”
眾所周知,許多腫瘤細胞的染色體數(shù)量會逐漸發(fā)生變化,其后果之一是癌細胞缺乏正確數(shù)量的遺傳物質(zhì)。
這些染色體變化在每個腫瘤中各不相同,但它們共同形成了染色體不穩(wěn)定性(CIN)的特征或標記。這項新研究基于這些CIN特征開發(fā)出生物標志物。
這些生物標志物讓我們能夠“提前檢測出哪些患者對這些治療具有耐藥性,這樣他們就可以避免不必要的副作用”,Macintyre解釋道。
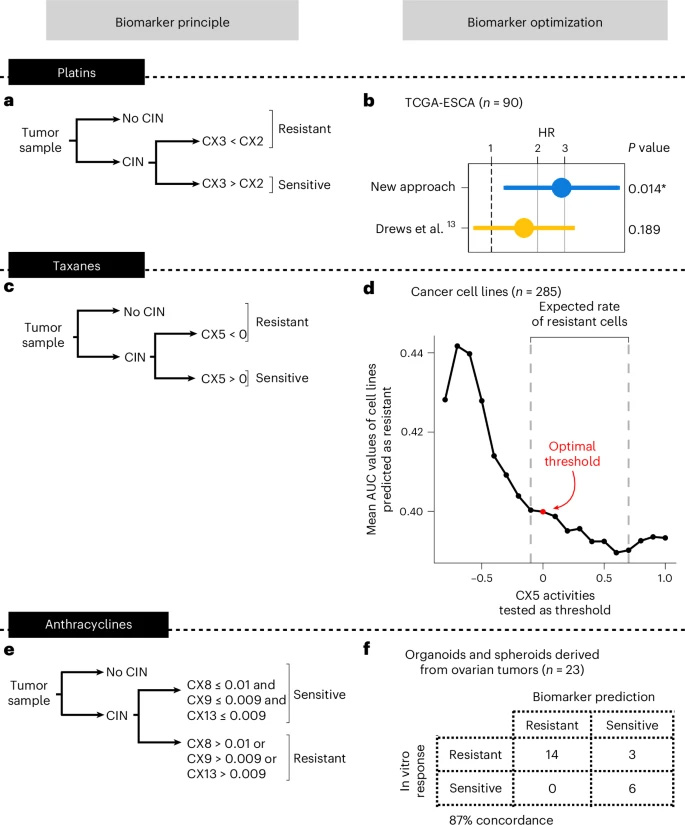
圖2 優(yōu)化用于預(yù)測泛癌種化療耐藥性的生物標志物
研究人員利用靶向捕獲基因組合測序、低深度全基因組測序和計算分析,以CIN特征為基礎(chǔ)來預(yù)測化療耐藥性。他們的分析聚焦于840名接受鉑類、紫杉類或蒽環(huán)類化療的癌癥患者。
這種方法擴展了人們對化療藥物作用機制的認識。例如,鉑類化療會引入較大的DNA加合物,而核苷酸切除修復(fù)功能受損的腫瘤難以修復(fù)這些加合物。此外,同源重組功能受損的腫瘤難以修復(fù)化療引起的雙鏈DNA斷裂。
研究人員隨后利用乳腺癌、卵巢癌、前列腺癌或肉瘤患者的回顧性數(shù)據(jù),在隨機對照臨床試驗中進行模擬。他們發(fā)現(xiàn),CIN標志物能夠揭示與三種化療引入的DNA損傷存在合成致死相互作用的突變是否存在。
具體來說,他們利用CIN標志物篩選出對紫杉類和蒽環(huán)類藥物存在耐藥風險的卵巢癌病例,以及對紫杉類或蒽環(huán)類化療耐藥風險增高的轉(zhuǎn)移性乳腺癌和前列腺癌病例。
研究人員表示:“這項研究結(jié)果強調(diào)了染色體不穩(wěn)定性特征在預(yù)測多種癌癥化療耐藥性方面的臨床價值,有望將‘一刀切’的化療方案轉(zhuǎn)變?yōu)榫珳实膫€性化治療。”
據(jù)Macintyre介紹,Tailor Bio公司是從劍橋大學(xué)分拆出來的,旨在基于這些CIN特征構(gòu)建精準醫(yī)學(xué)平臺。
“Tailor Bio打算將該檢測商業(yè)化,同時利用該技術(shù)對患者進行分層,以便嘗試新療法(例如通過與Volastra合作進行KIF18A抑制劑臨床試驗),” Macintyre說,并指出該公司也在針對染色體不穩(wěn)定的腫瘤開發(fā)治療方法。
參考資料
[1] Predicting resistance to chemotherapy using chromosomal instability signatures
摘要:研究團隊開發(fā)出一種方法,可以預(yù)測哪些患者不會對常用的化療藥物產(chǎn)生應(yīng)答。
化療是摧毀腫瘤細胞的一種策略。幾十年來,它一直是治療癌癥的標準方法。然而,化療并非總是有效。
西班牙國家癌癥研究中心(CNIO)計算腫瘤學(xué)團隊負責人Geoff Macintyre解釋說:“化療對某些患者有效,但并非適用于所有病例。20%到50%的癌癥患者對這些藥物沒有應(yīng)答。他們將承受化療帶來的副作用,卻無法獲得任何臨床收益。”
 圖1 利用染色體不穩(wěn)定性特征預(yù)測化療耐藥性
圖1 利用染色體不穩(wěn)定性特征預(yù)測化療耐藥性Macintyre領(lǐng)導(dǎo)的研究團隊與劍橋大學(xué)和初創(chuàng)公司Tailor Bio合作,開發(fā)出一種方法,可以預(yù)測哪些患者不會對常用的化療藥物(如鉑類、紫杉類和蒽環(huán)類化療藥物)產(chǎn)生應(yīng)答。
這項研究成果于6月23日發(fā)表在《Nature Genetics》雜志上。
作者表示: “重要的是,我們的研究為多種藥物引入了患者分層的生物標志物,這些藥物原本并不是作為靶向療法開發(fā)的。”
共同第一作者、西班牙國家癌癥研究中心的Joe Sneath Thompson表示:“我們的基因組檢測可以定量三種化療藥物的生物標志物。該檢測適用于多種不同類型的癌癥,因此,我們的研究成果每年有望惠及數(shù)十萬名患者。”
眾所周知,許多腫瘤細胞的染色體數(shù)量會逐漸發(fā)生變化,其后果之一是癌細胞缺乏正確數(shù)量的遺傳物質(zhì)。
這些染色體變化在每個腫瘤中各不相同,但它們共同形成了染色體不穩(wěn)定性(CIN)的特征或標記。這項新研究基于這些CIN特征開發(fā)出生物標志物。
這些生物標志物讓我們能夠“提前檢測出哪些患者對這些治療具有耐藥性,這樣他們就可以避免不必要的副作用”,Macintyre解釋道。

圖2 優(yōu)化用于預(yù)測泛癌種化療耐藥性的生物標志物
研究人員利用靶向捕獲基因組合測序、低深度全基因組測序和計算分析,以CIN特征為基礎(chǔ)來預(yù)測化療耐藥性。他們的分析聚焦于840名接受鉑類、紫杉類或蒽環(huán)類化療的癌癥患者。
這種方法擴展了人們對化療藥物作用機制的認識。例如,鉑類化療會引入較大的DNA加合物,而核苷酸切除修復(fù)功能受損的腫瘤難以修復(fù)這些加合物。此外,同源重組功能受損的腫瘤難以修復(fù)化療引起的雙鏈DNA斷裂。
研究人員隨后利用乳腺癌、卵巢癌、前列腺癌或肉瘤患者的回顧性數(shù)據(jù),在隨機對照臨床試驗中進行模擬。他們發(fā)現(xiàn),CIN標志物能夠揭示與三種化療引入的DNA損傷存在合成致死相互作用的突變是否存在。
具體來說,他們利用CIN標志物篩選出對紫杉類和蒽環(huán)類藥物存在耐藥風險的卵巢癌病例,以及對紫杉類或蒽環(huán)類化療耐藥風險增高的轉(zhuǎn)移性乳腺癌和前列腺癌病例。
研究人員表示:“這項研究結(jié)果強調(diào)了染色體不穩(wěn)定性特征在預(yù)測多種癌癥化療耐藥性方面的臨床價值,有望將‘一刀切’的化療方案轉(zhuǎn)變?yōu)榫珳实膫€性化治療。”
據(jù)Macintyre介紹,Tailor Bio公司是從劍橋大學(xué)分拆出來的,旨在基于這些CIN特征構(gòu)建精準醫(yī)學(xué)平臺。
“Tailor Bio打算將該檢測商業(yè)化,同時利用該技術(shù)對患者進行分層,以便嘗試新療法(例如通過與Volastra合作進行KIF18A抑制劑臨床試驗),” Macintyre說,并指出該公司也在針對染色體不穩(wěn)定的腫瘤開發(fā)治療方法。
參考資料
[1] Predicting resistance to chemotherapy using chromosomal instability signatures



