摘要:科學家合作,發現了由COVID-19引起的心臟炎癥、抗COVID-19疫苗接種和非COVID-19心肌炎的差異。
一組柏林研究人員與國際科學家合作,發現了由COVID-19引起的心臟炎癥、抗COVID-19疫苗接種和非COVID-19心肌炎的差異。他們在《自然心血管研究》上報告說,這一發現為更個性化的治療鋪平了道路。
心臟炎癥或心肌炎因病因而異。由柏林Max delbrck中心Norbert hbner教授的心血管疾病遺傳學和基因組學實驗室的科學家Henrike Maatz博士領導的一項合作研究發現,與非covid -19心肌炎相比,由SARS-CoV-2感染和mRNA疫苗引起的心肌炎具有獨特的免疫特征。這項研究發表在《自然心血管研究》雜志上。
 圖1 人類炎癥性心肌病在SARS-CoV-2感染和COVID-19疫苗接種后的細胞和分子心臟組織反應
圖1 人類炎癥性心肌病在SARS-CoV-2感染和COVID-19疫苗接種后的細胞和分子心臟組織反應“我們發現了免疫激活的明顯差異。這些知識可能有助于開發針對特定類型炎癥的新的、更個性化的治療方法。”Henrike Maatz博士說。
大流行期間的獨特機會
心肌炎是由各種類型的感染、自身免疫性疾病、遺傳和環境因素引起的,很少由疫苗接種引起。COVID-19主要是一種呼吸道疾病,但眾所周知,SARS-CoV-2感染會損傷心臟。在兒童和年輕人中,SARS-CoV-2感染可引起多系統炎癥綜合征,心肌炎是最普遍的臨床特征,盡管這種情況很少見。
當冠狀病毒大流行來臨時,Max delbrck中心、柏林慈善學院衛生研究所(BIH)和柏林慈善學院的研究人員看到了一個獨特的機會,可以研究心肌炎是否在細胞和分子水平上因病因而異。
Hübner實驗室長期以來一直對在單細胞水平上研究心臟病感興趣。他們與德國慈善中心(DHZC)的心臟病專家Carsten Tsch?pe教授合作,他是波黑免疫心臟病學研究小組的負責人,也是德國慈善中心(DZHK)的首席研究員。他的團隊一直在收集疑似心肌炎患者的活檢樣本。“在DHZC,我們有一個廣泛認可的心肌炎部門,專門在選定的病例中進行心內膜活檢,”Tsch?pe說。
“該學習項目是由慈善基金會在2019冠狀病毒病危機期間發起的,已被納入課程,成為DZHK支持的PERSONIFY項目的一部分。在此框架下,心肌炎患者接受高度特異性和針對性的調查,確保對其臨床和科學評估采用全面和先進的方法。”
Tsch?pe補充說:“我們非常感謝患者的信任和寶貴的貢獻,感謝我們的心力衰竭專科護士在識別患者、確保細致的數據管理、仔細的組織和血液處理以及全面的患者護理方面發揮的重要作用。”
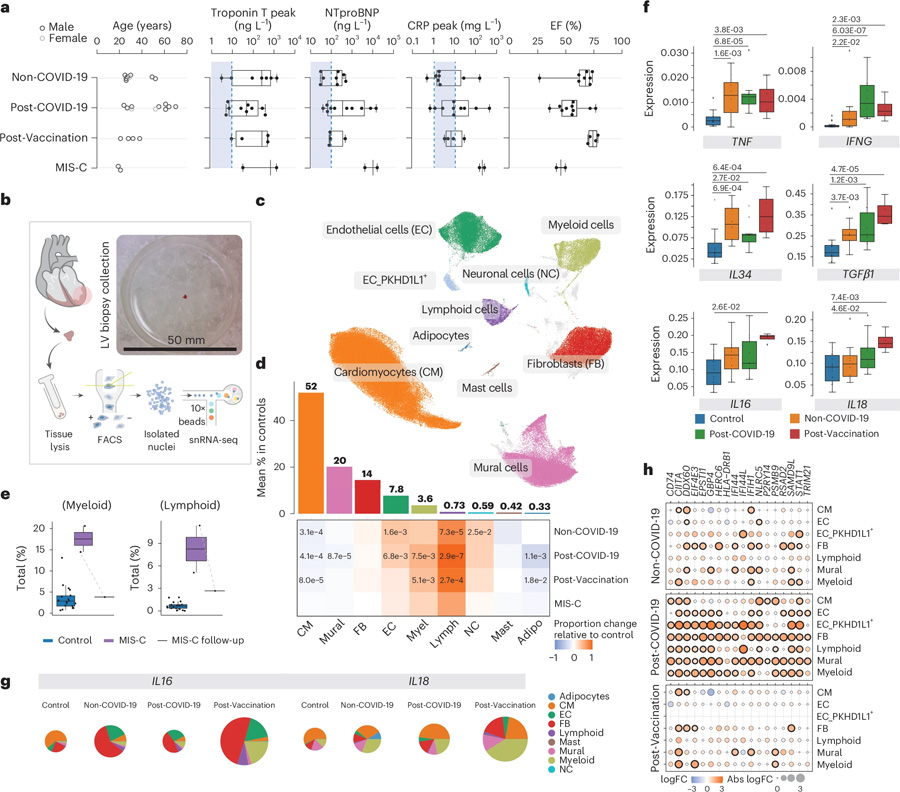
圖2 非COVID-19、COVID-19后以及疫苗接種后的炎癥性心肌病具有獨特的細胞和分子特征
明顯的免疫激活
Max delbrck中心的研究人員對活檢的心臟組織進行了單核RNA測序(snRNA-seq),以研究基因表達并創建每個細胞的轉錄譜。這些特征用于識別心臟的不同細胞類型。他們檢查了每個細胞的分子變化,以及三組不同心肌炎組織中不同細胞類型的豐度:COVID-19陽性樣本,mRNA疫苗引起的病例,以及大流行前病毒感染引起的非COVID-19心臟炎癥。
他們發現,雖然三組小鼠的一些基因表達變化相似,但免疫細胞基因表達水平存在顯著差異。更重要的是,轉錄譜還顯示,免疫細胞的豐度不同,這取決于心肌炎的病因。
這樣的差異是出乎意料的,例如,研究人員發現,接種疫苗后,CD4 T細胞更豐富,而感染SARS-CoV-2后,CD8 T細胞往往更占優勢。在非covid -19心肌炎樣本中,CD4細胞與CD8細胞的比例約為50/50。基因表達數據表明,covid -19后組的CD8 T細胞也比非covid -19心肌炎組更具侵襲性。研究人員還發現,在COVID-19后心肌炎中存在一小群T細胞,這些細胞以前只在COVID-19重癥患者的血液中觀察到。
“總之,這些發現表明,與大流行前的心肌炎相比,covid -19后心肌炎的免疫反應更強,而接種疫苗后的心肌炎癥似乎更溫和,”盡管疫苗接種后心肌炎患者的樣本量很小,但結果與其他疫苗接種后心肌炎的研究一致。
對治療的啟示
Maatz說,能夠區分由不同類型的感染和疫苗接種引起的炎癥,為改善針對特定類型炎癥的治療鋪平了道路。例如,她補充說,基于這項研究,人們可以開發新的療法來控制疫苗的副作用。
此外,心臟的活檢樣本通常很小——它們沒有針頭大。Maatz說,讓snRNA-seq技術在如此少量的組織中發揮作用是一個挑戰。“但我認為,我們能夠產生的分辨率和洞察力的深度真正顯示了這種方法的力量,也許將來也可以用于診斷環境。”
參考資料
[1] The cellular and molecular cardiac tissue responses in human inflammatory cardiomyopathies after SARS-CoV-2 infection and COVID-19 vaccination
摘要:科學家合作,發現了由COVID-19引起的心臟炎癥、抗COVID-19疫苗接種和非COVID-19心肌炎的差異。
一組柏林研究人員與國際科學家合作,發現了由COVID-19引起的心臟炎癥、抗COVID-19疫苗接種和非COVID-19心肌炎的差異。他們在《自然心血管研究》上報告說,這一發現為更個性化的治療鋪平了道路。
心臟炎癥或心肌炎因病因而異。由柏林Max delbrck中心Norbert hbner教授的心血管疾病遺傳學和基因組學實驗室的科學家Henrike Maatz博士領導的一項合作研究發現,與非covid -19心肌炎相比,由SARS-CoV-2感染和mRNA疫苗引起的心肌炎具有獨特的免疫特征。這項研究發表在《自然心血管研究》雜志上。
 圖1 人類炎癥性心肌病在SARS-CoV-2感染和COVID-19疫苗接種后的細胞和分子心臟組織反應
圖1 人類炎癥性心肌病在SARS-CoV-2感染和COVID-19疫苗接種后的細胞和分子心臟組織反應“我們發現了免疫激活的明顯差異。這些知識可能有助于開發針對特定類型炎癥的新的、更個性化的治療方法。”Henrike Maatz博士說。
大流行期間的獨特機會
心肌炎是由各種類型的感染、自身免疫性疾病、遺傳和環境因素引起的,很少由疫苗接種引起。COVID-19主要是一種呼吸道疾病,但眾所周知,SARS-CoV-2感染會損傷心臟。在兒童和年輕人中,SARS-CoV-2感染可引起多系統炎癥綜合征,心肌炎是最普遍的臨床特征,盡管這種情況很少見。
當冠狀病毒大流行來臨時,Max delbrck中心、柏林慈善學院衛生研究所(BIH)和柏林慈善學院的研究人員看到了一個獨特的機會,可以研究心肌炎是否在細胞和分子水平上因病因而異。
Hübner實驗室長期以來一直對在單細胞水平上研究心臟病感興趣。他們與德國慈善中心(DHZC)的心臟病專家Carsten Tsch?pe教授合作,他是波黑免疫心臟病學研究小組的負責人,也是德國慈善中心(DZHK)的首席研究員。他的團隊一直在收集疑似心肌炎患者的活檢樣本。“在DHZC,我們有一個廣泛認可的心肌炎部門,專門在選定的病例中進行心內膜活檢,”Tsch?pe說。
“該學習項目是由慈善基金會在2019冠狀病毒病危機期間發起的,已被納入課程,成為DZHK支持的PERSONIFY項目的一部分。在此框架下,心肌炎患者接受高度特異性和針對性的調查,確保對其臨床和科學評估采用全面和先進的方法。”
Tsch?pe補充說:“我們非常感謝患者的信任和寶貴的貢獻,感謝我們的心力衰竭專科護士在識別患者、確保細致的數據管理、仔細的組織和血液處理以及全面的患者護理方面發揮的重要作用。”

圖2 非COVID-19、COVID-19后以及疫苗接種后的炎癥性心肌病具有獨特的細胞和分子特征
明顯的免疫激活
Max delbrck中心的研究人員對活檢的心臟組織進行了單核RNA測序(snRNA-seq),以研究基因表達并創建每個細胞的轉錄譜。這些特征用于識別心臟的不同細胞類型。他們檢查了每個細胞的分子變化,以及三組不同心肌炎組織中不同細胞類型的豐度:COVID-19陽性樣本,mRNA疫苗引起的病例,以及大流行前病毒感染引起的非COVID-19心臟炎癥。
他們發現,雖然三組小鼠的一些基因表達變化相似,但免疫細胞基因表達水平存在顯著差異。更重要的是,轉錄譜還顯示,免疫細胞的豐度不同,這取決于心肌炎的病因。
這樣的差異是出乎意料的,例如,研究人員發現,接種疫苗后,CD4 T細胞更豐富,而感染SARS-CoV-2后,CD8 T細胞往往更占優勢。在非covid -19心肌炎樣本中,CD4細胞與CD8細胞的比例約為50/50。基因表達數據表明,covid -19后組的CD8 T細胞也比非covid -19心肌炎組更具侵襲性。研究人員還發現,在COVID-19后心肌炎中存在一小群T細胞,這些細胞以前只在COVID-19重癥患者的血液中觀察到。
“總之,這些發現表明,與大流行前的心肌炎相比,covid -19后心肌炎的免疫反應更強,而接種疫苗后的心肌炎癥似乎更溫和,”盡管疫苗接種后心肌炎患者的樣本量很小,但結果與其他疫苗接種后心肌炎的研究一致。
對治療的啟示
Maatz說,能夠區分由不同類型的感染和疫苗接種引起的炎癥,為改善針對特定類型炎癥的治療鋪平了道路。例如,她補充說,基于這項研究,人們可以開發新的療法來控制疫苗的副作用。
此外,心臟的活檢樣本通常很小——它們沒有針頭大。Maatz說,讓snRNA-seq技術在如此少量的組織中發揮作用是一個挑戰。“但我認為,我們能夠產生的分辨率和洞察力的深度真正顯示了這種方法的力量,也許將來也可以用于診斷環境。”
參考資料
[1] The cellular and molecular cardiac tissue responses in human inflammatory cardiomyopathies after SARS-CoV-2 infection and COVID-19 vaccination



